Mục lục
Axit sunfuric (H2SO4) được mệnh danh là “vua” của các loại hóa chất, được sử dụng rộng rãi trong nhiều ngành công nghiệp và ứng dụng đời sống hiện nay. Vậy thực chất H2SO4 là gì mà lại có sức ảnh hưởng lớn đến thế? Hãy cùng D.A.P Chem đi tìm kiếm câu trả lời trong bài viết dưới nhé!
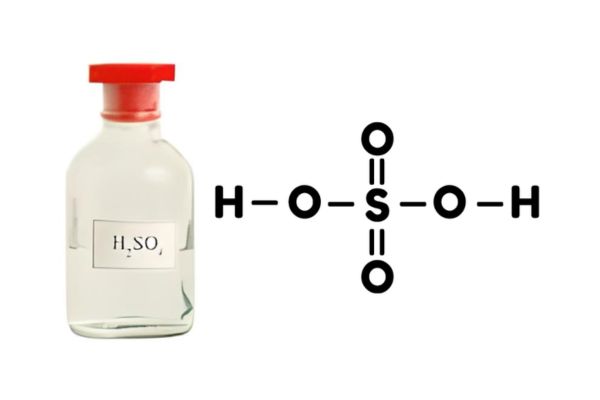
H2SO4 là gì?
Nhiều người thường thắc mắc “H2SO4 là chất gì?” Câu trả lời là axit sunfuric, một loại axit vô cơ mạnh với công thức hóa học H2SO4. Axit sunfuric bao gồm các nguyên tố lưu huỳnh, oxy và hydro, tồn tại dưới dạng chất lỏng không màu, không mùi, sánh và nặng hơn nước. Khi hòa tan trong nước sẽ tỏa ra một lượng nhiệt rất lớn.
Cấu tạo phân tử
Công thức phân tử: H2SO4
Công thức cấu tạo của H2SO4:
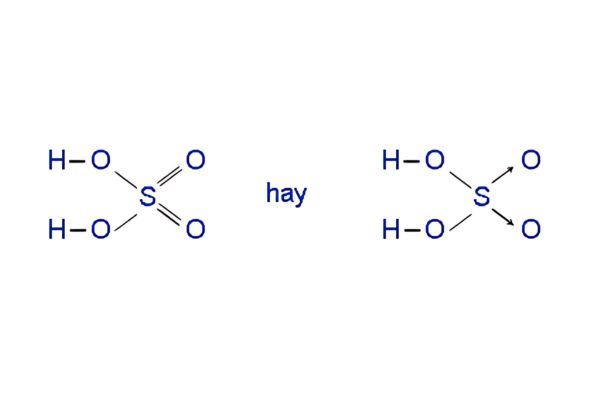
Mô hình phân tử H2SO4:
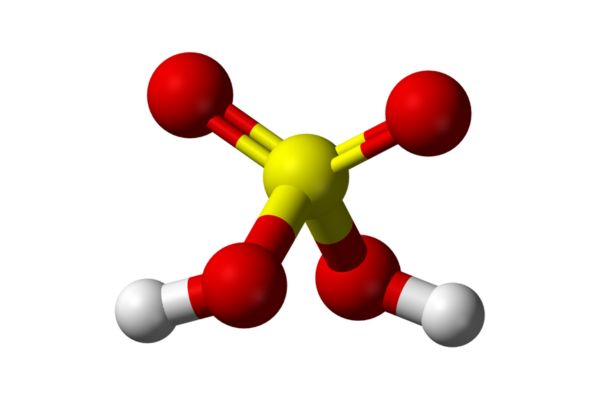
Tính chất vật lý
- Axit sunfuric là chất lỏng không màu, dạng sánh hơi nhớt, nặng hơn nước, khó bay hơi và tan vô hạn trong nước.
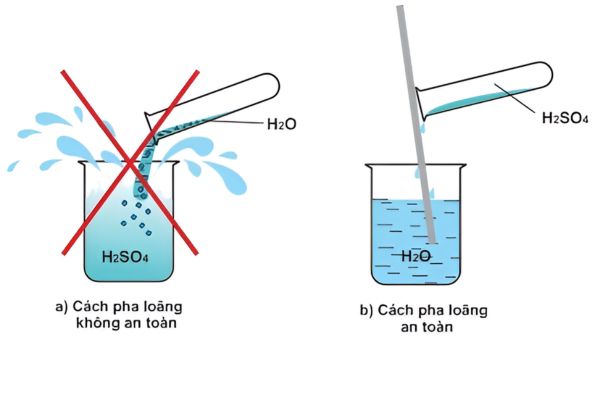
- Axit sunfuric đặc rất háo nước và tỏa nhiều nhiệt. Khi pha loãng phải cho từ từ H2SO4 đặc vào nước và tuyệt đối không làm ngược lại để tránh gây bỏng.
- Axit sunfuric đặc có khả năng biến nhiều hợp chất hữu cơ thành than.

Tính chất hóa học
Axit sunfuric có hai dạng chính: axit sunfuric loãng và axit sunfuric đặc, mỗi dạng có những tính chất hóa học khác nhau.
1. Axit sunfuric loãng
Axit sunfuric là một axit mạnh và sở hữu đầy đủ các tính chất hóa học đặc trưng của axit, bao gồm:
- H2SO4 chuyển màu quỳ tím thành đỏ.
- H2SO4 loãng tác dụng với kim loại đứng trước Hydro (trừ Chì – viết tắt là Pb) tạo thành muối sunfat.
Fe + H2SO4 → FeSO4 + H2
- H2SO4 loãng tác dụng với oxit bazo tạo thành muối mới và nước.
FeO + H2SO4 → FeSO4 + H2O
- H2SO4 loãng tác dụng với bazo tạo thành muối mới và nước.
H2SO4 + NaOH → NaHSO4 + H2O
H2SO4 + 2NaOH → Na2SO4 + 2H2O
- H2SO4 loãng tác dụng với muối tạo thành muối mới và axit mới.
H2SO4 + 2KHCO3 → K2SO4 + 2H2O + 2CO2
2. Axit sunfuric đặc
Axit sunfuric đặc có tính axit mạnh và khả năng oxi hóa cao với các đặc tính hóa học nổi bật như:
- H2SO4 đặc tác dụng với kim loại: Khi cho mảnh đồng (Cu) vào axit sunfuric (H2SO4), tạo ra dung dịch màu xanh và có khí bay lên với mùi sốc.
2H2SO4 + Cu → CuSO4 + SO2 + 2H2O
- H2SO4 đặc tác dụng với phi kim tạo thành oxit phi kim + H2O + SO2.
C + 2H2SO4 → CO2 + 2H2O + 2SO2 (nhiệt độ)
2P + 5H2SO4 → 2H3PO4 + 5SO2 + 2H2O
- H2SO4 đặc tác dụng với các chất khử khác.
2FeO + 4H2SO4 → Fe2(SO4)3 + SO2 + 4H2O
- H2SO4 có tính háo nước mạnh: Khi đưa H2SO4 vào cốc đựng đường, sau phản ứng đường bị chuyển sang màu đen và xảy ra hiện tượng phun trào.
C12H22O11 + H2SO4 → 12C + H2SO4.11H2O
Điều chế axit sunfuric (H2SO4)
Thông thường, H2SO4 được sản xuất bằng cách đốt quặng pirit (FeS2) để tạo ra SO2. Sau đó, SO2 được oxy hóa thành SO3 trong điều kiện nhiệt độ 400-500°C. Cuối cùng, SO3 được hòa tan trong nước để tạo ra axit sunfuric, thường bằng cách pha loãng oleum với lượng nước thích hợp.
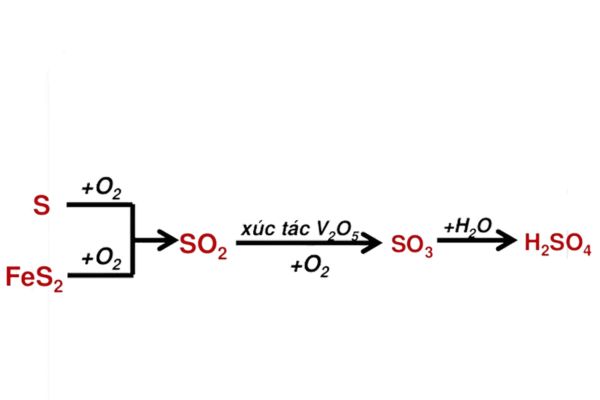
Các dạng của axit sunfuric H2SO4
Mặc dù có thể sản xuất axit sunfuric tinh khiết 100% nhưng nó sẽ mất SO3 khi đến điểm sôi, dẫn đến sản phẩm có nồng độ khoảng 98,3%. Các nồng độ khác nhau của axit sunfuric được sử dụng cho các mục đích khác nhau như sau:
- H2SO4 loãng với nồng độ 10% thường được sử dụng trong phòng thí nghiệm.
- H2SO4 với nồng độ 33,5% được dùng trong ắc quy.
- H2SO4 với nồng độ 62,18% được sử dụng trong sản xuất phân bón.
- Nồng độ 77,67% được dùng trong các tháp sản xuất và axit Glover.
- Nồng độ 98% là axit sunfuric đậm đặc.
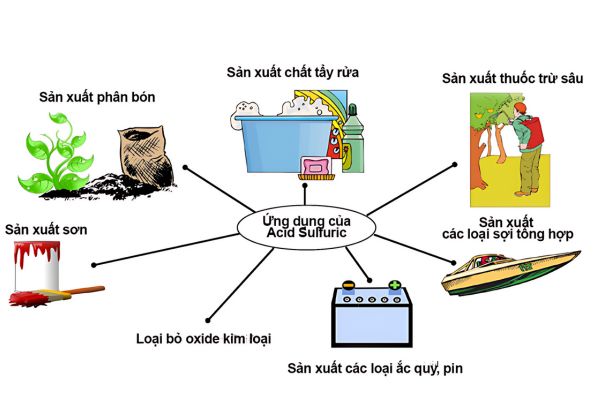
Ứng dụng của hóa chất H2SO4 trong đời sống
Axit sunfuric là hóa chất hàng đầu, được ứng dụng nhiều trong đời sống với vai trò nguyên liệu chính hay chất xúc tác.
1. Trong sản xuất phân bón
Axit sunfuric được sử dụng chủ yếu để sản xuất axit photphoric, nguyên liệu quan trọng trong sản xuất phân photphat và amoni sunfat. Chất này có mặt trong đa số các loại phân bón hiện có trên thị trường hiện nay.
2. Trong sản xuất công nghiệp
- H2SO4 được dùng để sản xuất kim loại như đồng và kẽm,… làm sạch bề mặt thép và loại bỏ gỉ sét.
- Sử dụng để sản xuất nhôm sunfat (phèn làm giấy), các muối sunfat, thuốc nổ, thuốc nhuộm, chất dẻo và dược phẩm.
- Hỗn hợp H2SO4 với nước được dùng làm chất điện giải trong ắc quy, axit chì.
- Mỗi năm có khoảng 160 triệu tấn H2SO4 được tiêu thụ, chủ yếu trong sản xuất phân bón (30%), chất tẩy rửa (14%), giấy và sợi (8%), chất dẻo (5%), luyện kim (2%) và phẩm nhuộm (2%).
3. Trong xử lý nước thải
Axit sunfuric được sử dụng để sản xuất nhôm hidroxit, một chất quan trọng trong các nhà máy xử lý nước. Nhôm hidroxit giúp lọc tạp chất, cải thiện mùi vị nước, trung hòa độ pH và loại bỏ các ion Ca²⁺ và Mg²⁺ trong nước thải.
4. Trong phòng thí nghiệm
Axit sunfuric là hợp chất đậm đặc được dùng để điều chế các axit yếu hơn như HNO3 và HCl trong các thí nghiệm. Ngoài ra, H2SO4 tham gia vào nhiều phản ứng hóa học với các chất khác để tạo ra sản phẩm phục vụ cho sự phát triển kinh tế và quân sự.
5. Một số ứng dụng khác của axit sunfuric
Ứng dụng của H2SO4 trong đời sống rất đa dạng. Ngoài các ứng dụng đã đề cập, H2SO4 còn được sử dụng trong các lĩnh vực khác như:
- Ứng dụng axit sunfuric làm sạch cống rãnh
- Ứng dụng axit sunfuric làm bột giặt từ phản ứng hóa học với axit sunfuric (60% sản lượng toàn cầu) tạo ra natri photphoric.
- Ứng dụng axit sunfuric làm chất xúc tác cho phản ứng giữa isobutan và isobutylen để tạo ra chất isooctan trong ngành hóa dầu.
Lưu ý khi sử dụng và cách bảo quản H2SO4
Khi sử dụng và bảo quản axit sunfuric (H2SO4), cần tuân thủ các lưu ý quan trọng dưới đây để đảm bảo an toàn và hiệu quả.

Những lưu ý khi sử dụng H2SO4
- Khi pha loãng axit sunfuric, hãy thêm từ từ axit vào nước và khuấy đều. Tuyệt đối không làm ngược lại để tránh gây bỏng.
- Axit sunfuric là chất nguy hiểm. Tránh tiếp xúc trực tiếp với da và mắt vì có thể gây bỏng và tổn thương vĩnh viễn.
- Khi sử dụng hoặc bơm H2SO4, cần mặc quần áo bảo hộ và đeo mặt nạ chuyên dụng để bảo vệ mắt, đặc biệt phải dùng vật chứa được cấp phép an toàn khi vận chuyển.
- Tránh để H2SO4 chảy vào hệ thống thoát nước.
- Nếu xảy ra rò rỉ, cách ly khu vực nguy hiểm và đảm bảo chỉ những người có bảo hộ mới được vào.
- Sử dụng thanh chắn nhựa hoặc rãnh bảo vệ để ngăn chặn axit tràn ra ngoài.
Lưu ý khi bảo quản
- Đậy kín nắp và bảo quản axit sunfuric ở nơi khô ráo, tránh xa các chất bazơ và chất khử.
- Sử dụng dụng cụ bằng nhựa để chứa axit sunfuric. Tránh dùng các bồn chứa làm từ nhôm, thép, inox hoặc kẽm vì axit có tính ăn mòn cao, ngay cả khi pha loãng. Nếu dùng thùng sắt, cần tráng một lớp sơn PU bên trong.
- Không để axit sunfuric gần kim loại nhẹ hoặc các chất có tính axit như HCl, acid nitric (HNO3), acid phosphoric (H3PO4) để ngăn ngừa nguy cơ cháy nổ và nguy hiểm.
Lựa chọn mua hóa chất sunfuric chất lượng tại đâu?
DAP Chemical là thương hiệu cung ứng thiết bị, hóa chất chuyên dụng uy tín hàng đầu tại Việt Nam. Đến với Công ty DAP, bạn có thể tìm thấy các sản phẩm axit chất lượng cao như axit clohiđric, axit sunfuric loãng và nhiều loại hóa chất khác. Các sản phẩm tại đây đều được kiểm định và cấp phép lưu hành trên thị trường, đảm bảo an toàn và đáng tin cậy cho người sử dụng.

Hy vọng bài viết này đã giúp bạn giải đáp câu hỏi “H2SO4 là gì?” và cung cấp góc nhìn sâu hơn về đặc điểm, tính chất cũng như ứng dụng của axit sunfuric trong đời sống. Nếu bạn đang cần mua các loại sản phẩm axit, hãy liên hệ ngay với Công ty DAP Chem để được tư vấn, báo giá và đặt hàng nhanh chóng!
Thông tin liên hệ:
Địa chỉ: CL 18-29 Khu đất dịch vụ La Dương, đường La Nội, Phường Dương Nội, Quận Hà Đông, Thành Phố Hà Nội
Điện thoại: 0833 698 989
Website: Dapchem.com

